計画名
新規尿中バイオマーカーによる尿路上皮がん検査システムの開発・事業化
申請区分:(H)従来にはない革新的な診断や高度化された画像・光学診断の実現
事業概要
現在、尿路上皮がんの確定診断には肉体的・精神的な苦痛を伴う膀胱鏡検査が必須であるため、信頼性の高い予備診断法が必要となっている。この課題を解決するために、新たな尿路上皮がんの検査方法を提案する。従来の尿細胞診+膀胱鏡検査を実施するフローから尿細胞診+新規バイオマーカー検査を予備診断として陽性の場合のみ膀胱鏡検査を実施するという新たなフローへの変更により、膀胱鏡検査の頻度を減らすことで患者負担を大きく低減させることを目指している。
また、バイオセンサにより小型で安価な検査システムを実現する。これにより、小規模医療機関でも検査が可能となり、患者の検診負担を軽減すると共に、大病院への患者集中の緩和や泌尿器科専門医が不足する医療過疎地域対策にも貢献することが期待される。
事業化する医療機器等の概要
事業コンセプト

基本情報
| 製品名 | 未定 | 一般的名称 | 該当なし |
| クラス分類 | クラスⅢ(想定) | 許認可区分 | 承認(想定) |
| 申請区分 | 改良(想定) | 承認・認証番号等 | ー |
| 薬事申請予定者 | 京セラ株式会社 | 製造販売業許可 | 取得済み |
上市予定
| | 国内市場 | 海外市場(米国・欧州) |
| 薬事申請時期 | 2026年 | 非公開 |
| 上市時期 | 2027年 | 非公開 |
事業成果
| 令和4年度 | 令和5年度 | 令和6年度 | 令和7年度 | 令和8年度 | 令和9年度 | 事業化製品 |
|---|
| 成果報告 | - | - | - | - | - | - |
コンソーシアム体制
実証事業コンソーシアム構成イメージ
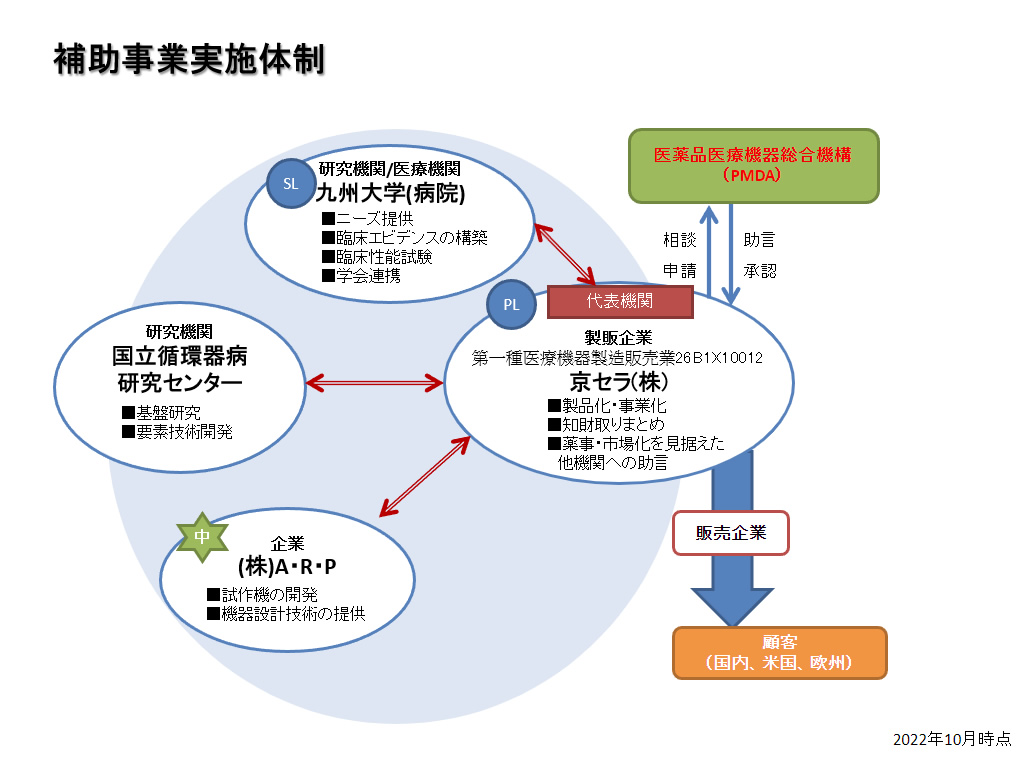
実証事業コンソーシアム構成メンバー
| 代表機関 | 分担機関 |
| 京セラ株式会社 | 九州大学、国立循環器病研究センター、株式会社A・R・P |



