【管理番号30-218】 膝前十字靭帯再建に用いる脱細胞化組織由来の医療機器開発・海外展開
計画名
膝前十字靭帯再建に用いる脱細胞化組織由来の医療機器開発・海外展開
申請区分: 海外市場獲得
事業概要
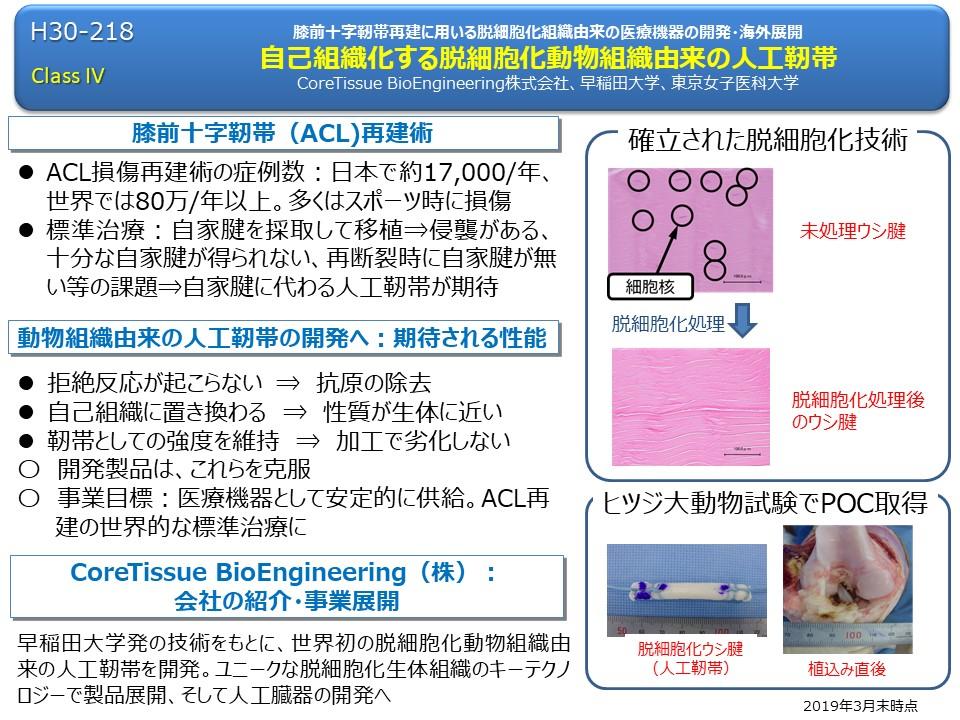
膝前十字靭帯(ACL)再建術では、自家腱を採取して移植する治療が標準であるが、侵襲等の課題から、自家腱を採取せずに再建術が行える人工靭帯が待ち望まれている。
本課題は、安定供給可能で、生体適合性が高く、再建時に十分な強度を有する人工靭帯として、動物(ウシ)の腱を出発材料とし、独自の脱細胞化処理と滅菌処理を施し、再建後に体内で自己組織化するACL再建術用の人工靭帯を開発し、国内外にて事業展開することである。
事業化する医療機器等の概要
事業コンセプト
基本情報
| 製品名 | 自己組織化人工靭帯(膝前十字靭帯再建用) | 一般的名称 | (新設案:ウシ腱組織使用人工靭帯) |
|---|---|---|---|
| クラス分類 | クラスⅣ | 許認可区分 | 承認 |
| 申請区分 | 新医療機器 | 承認・認証番号等 | - |
| 薬事申請予定者 | CoreTissue BioEngineering株式会社 | 製販業許可 | 取得予定 |
上市予定
| 国内市場 | 海外市場(具体的に:米国) | |
|---|---|---|
| 薬事申請時期 | 2023年 | 2023年 |
| 上市時期 | 2025年 | 2025年 |
事業成果
コンソーシアム体制
実証事業コンソーシアム構成イメージ
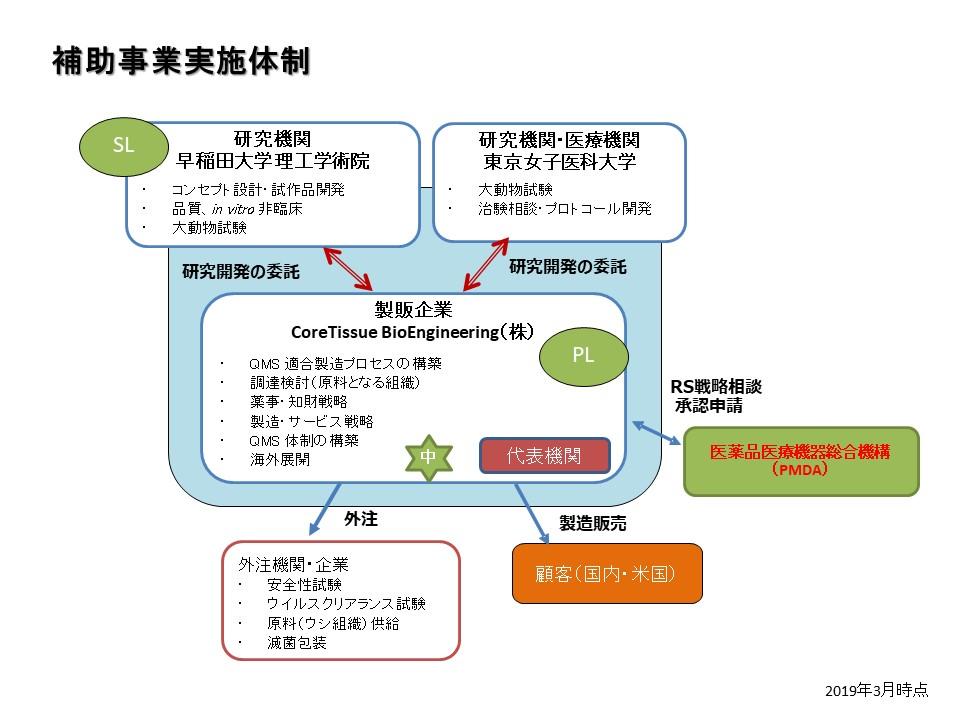
実証事業コンソーシアム構成メンバー
| 代表機関 | 分担機関 |
|---|---|
| CoreTissue BioEngineering株式会社 | 学校法人早稲田大学 学校法人東京女子医科大学 |

