【管理番号28-020】胎児由来の羊膜再利用によるハイパードライ(HD)羊膜の開発・海外展開
計画名
胎児由来の羊膜再利用によるハイパードライ(HD)羊膜の開発・海外展開
申請区分: 海外市場の獲得
事業概要
日本国内ではヒト由来原材料由来の製品化の前例がなく、規制の観点で製品化に多大な時間とコストを要する。従って、本事業では既に市場が確立されている米国市場に対して、Hyper-Dry製法にて生産した乾燥羊膜の製品化を速やかに行う(創傷被覆・眼科領域:治験不要のため短期間で上市可能)。
具体的には、生羊膜の調達、及びHyper-Dry乾燥・生産工程は日本国内で構築し、新設した国内自社工場で生産したHD羊膜の米国輸出・販売に向けた事業化を図る。
事業化する医療機器等の概要
事業コンセプト
基本情報
| 製品名 | HD羊膜(予定) | 一般的名称 | 創傷被覆・保護材(生物由来材料) |
|---|---|---|---|
| クラス分類 | 361 HCT/P | 許認可区分 | 届出 |
| 申請区分 | 後発医療機器 | 承認・認証番号等 | - |
| 薬事申請予定者 | 株式会社アムノス | 製販業許可 | 取得済み |
上市予定
| 国内市場(参考) | 海外市場(具体的に:米国) | |
|---|---|---|
| 薬事申請時期 | 2022年 | 2018年 |
| 上市時期 | 2023年 | 2018年 |
事業成果
コンソーシアム体制
実証事業コンソーシアム構成イメージ
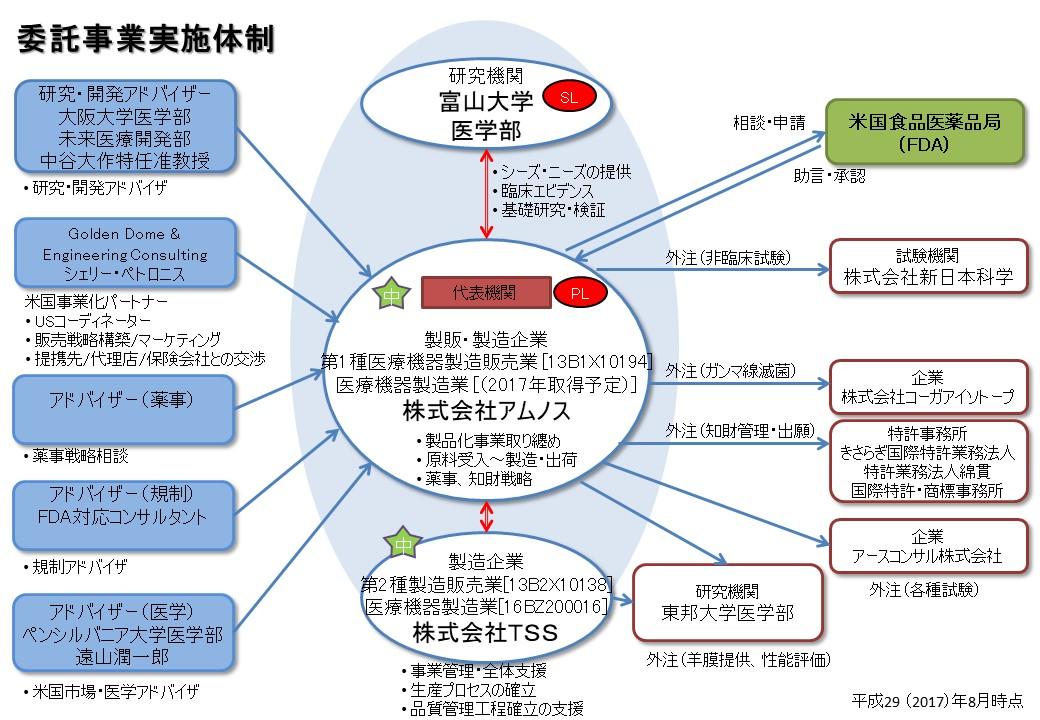
実証事業コンソーシアム構成メンバー
| 代表機関 | 分担機関 |
|---|---|
| 株式会社アムノス | 国立大学法人富山大学 株式会社TSS |

